Les organoïdes, un outil complémentaire à l’expérimentation animale
La recherche employant des organes «minimalistes» prend de l’ampleur à l’UNIL. Ces nouveaux systèmes d’étude offrent une approche pour Réduire, Remplacer, Raffiner l'utilisation d'animaux. Dialogue croisé autour des organoïdes entre la professeure Claudia Bagni du Département des neurosciences fondamentales et la professeure Tatiana Petrova du Département d’oncologie fondamentale.
Les organoïdes sont des outils d’expérimentation scientifique en cours de développement dans plusieurs départements de l’UNIL et du CHUV, notamment dans les domaines des neurosciences fondamentales, cliniques et psychiatriques, des sciences biomédicales, de l’oncologie et de l’ophtalmologie. Pour promouvoir cette technologie, la Faculté de biologie et de médecine (FBM) va se doter d’équipements de pointe pour l’imagerie, la culture et le séquençage d'organoïdes, grâce au soutien de la Direction de l’UNIL. Étendre l’usage des méthodes dites alternatives à l’expérimentation animale contribuera à augmenter l’ancrage des principes des 3R. La professeure Claudia Bagni du Département des neurosciences fondamentales, et future vice-Doyenne à la FBM, et la professeure Tatiana Petrova du Département d’oncologie fondamentale, sont en charge de développer l’utilisation des organoïdes à l’UNIL. Elles soulignent que ce projet a été alimenté par le désir des scientifiques lausannois·es de Réduire, Remplacer, Raffiner (3R) l'utilisation d'animaux dans la recherche.
Que se cache-t-il derrière ces mini-organes?
Claudia Bagni (C.B.): Il s’agit d’un système fascinant qui permet de comprendre les premières étapes du développement d'un organe et offre un potentiel à l'étude des maladies humaines. À la différence de la culture cellulaire classique en mono-couche, un organoïde est un regroupement de plusieurs couches de différents types de cellules, qui se développe en trois dimensions (3D) et crée un tissu cellulaire.
Tatiana Petrova (T.P.): L’organisation de presque tous les organes, tels que le foie, le cerveau, l’intestin, les reins, la prostate, le pancréas, etc., peut être mimée. Cependant, nous sommes toutes deux d’accord pour ne pas appeler ces structures des mini-foies ou des mini-cerveaux, car ces dernières ne sont pas aussi complètes qu’un organe grandeur nature.
Comment les obtient-on en laboratoire?
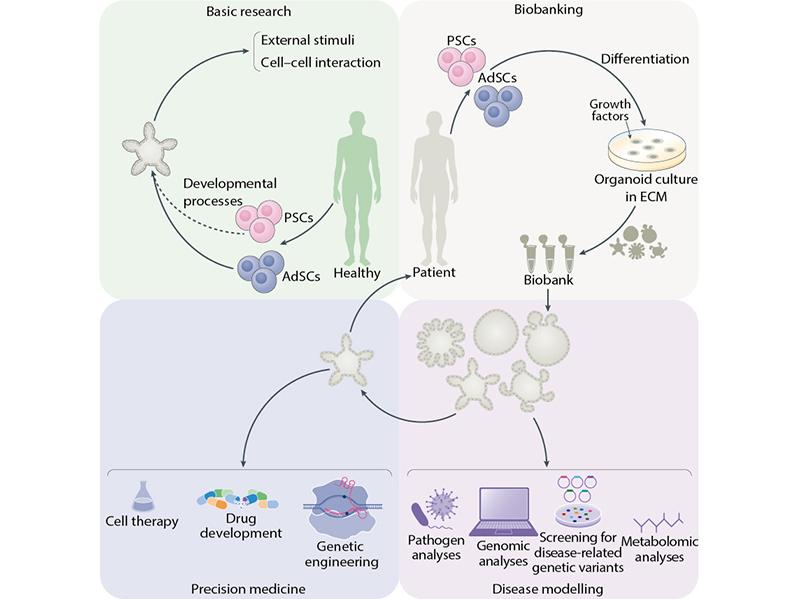
T.P.: Il y a deux méthodes principales. La première technique emploie directement des cellules souches de tissus spécialisés, alors que la seconde approche est indirecte. En effet, des cellules adultes différenciées sont isolées à partir d’un tissu, puis reprogrammées génétiquement en cellules immatures qui peuvent devenir n’importe quel type de cellule. Elles sont appelées en anglais iPSC, pour cellules souches à pluripotence induite. Dans les deux méthodes, la présence de facteurs de croissance spécifiques et la culture en 3D permettent ensuite à ces unités de se différencier et se multiplier pour créer un groupe de cellules, un organoïde. Ce dernier peut être maintenu en culture ou congelé pour une exploitation ultérieure.
C.B.: Le procédé des mini-organes n’aurait pas vu le jour sans la découverte du fait que les cellules matures peuvent être reprogrammées pour devenir pluripotentes (iPSC). Les chercheurs John B. Gurdon et Shinya Yamanaka ont reçu le prix Nobel de physiologie ou de médecine en 2012 pour leurs contributions révolutionnaires, en 1962 et 2008 respectivement, dans le domaine de la reprogrammation cellulaire. La génération d'organoïdes a de vastes implications thérapeutiques, en particulier dans le contexte de la modélisation in vitro des maladies, du criblage pharmaceutique et de la médecine de précision.
Qu’est-il possible d’étudier grâce à l’utilisation d’organoïdes et d’iPSC?
C.B.: D'une part, la formation d'un organoïde étant fondée sur le mouvement des cellules, comme c'est le cas des organes dans le corps humain, nous sommes en mesure de suivre la communication entre cellules dans un contexte plus physiologique car basé sur des forces mécaniques. D'autre part, le maniement des iPSC et des organoïdes permet aux chercheur·euse·s biomédicaux de mieux comprendre les étapes précoces des maladies neurodégénératives, telles que la maladie d'Alzheimer, ou des troubles du développement neurologique, comme l'autisme.
T.P.: En oncologie, l’espoir majeur est de développer des traitements personnalisés. Des organoïdes dérivés à partir d’une tumeur d’un·e patient·e peuvent servir à tester des médicaments, individuels ou en combinaison, afin d’anticiper la sensibilité ou la résistance de ce·tte patient·e aux thérapies disponibles.
C.B.: Les iPSC humaines et les organoïdes permettront d’enrichir la médecine personnalisée dans de nombreux champs médicaux, de compléter les systèmes modèles existants et d’étendre la découverte de médicaments à un environnement plus conforme à la physiologie humaine.
Quelles sont les limitations des organes miniatures?
C.B.: Ce sont des tissus isolés. Par conséquent, toutes les questions biomédicales ne peuvent être investiguées avec cet outil révolutionnaire. Par exemple, la recherche sur le comportement ou encore sur la plasticité d’un cerveau de taille réelle ne peut être réalisée avec les organoïdes.
T.P.: En cancérologie, la complexité du microenvironnement n’y est pas reproduite à l’identique. Prenons le cas d’un organoïde de tumeur de colon. Malgré la présence de cellules cancéreuses, il manque les cellules immunitaires, mais aussi d’autres types cellulaires tels que les fibroblastes ou les cellules endothéliales, qui jouent un rôle essentiel dans les tumeurs in vivo. Heureusement, grâce à la coculture, nous pouvons partiellement pallier cet inconvénient en ajoutant à ce mini-organe quelques coéquipiers cellulaires absents.
Que va permettre l’acquisition d’une panoplie de nouveaux instruments à la FBM?
C.B.: Ces équipements sophistiqués offriront la possibilité d’effectuer des criblages à haut débit, c’est-à-dire des essais d’un grand nombre de composés biologiques ou chimiques de manière automatisée, dans un contexte plus physiologique (en 3D et en mouvement) qu’avec de la simple culture cellulaire. L’analyse intégrée des effets de ces molécules sur une maladie pourra être réalisée à différentes échelles – moléculaire (analyse de l’expression de gènes) et cellulaire (enregistrement de courants électriques) – et couplée à de la visualisation (grâce à l’imagerie).
T.P.: De plus, le passage au crible de médicaments sur les organoïdes remplacera quelques expériences sur l’animal. En l’absence d’efficacité, des molécules seront alors écartées, réduisant ainsi le nombre nécessitant une validation in vivo. Cette méthode, dite alternative, est complémentaire à l’expérimentation animale, qui ne peut donc pas être totalement abandonnée. Toutefois, l’usage des organoïdes permet de réduire le nombre d’expériences in vivo.
C.B.: Malgré les nombreux avantages détaillés ci-dessus, la culture d'organoïdes humains est encore en développement, et de nombreux efforts pour faire progresser cette technologie sont toujours en cours. Avec le soutien de la Direction de l’UNIL, nous envisageons de faire passer la recherche sur les organoïdes à la vitesse supérieure. Une telle plateforme technologique permettra de renforcer les collaborations intra- et inter-départements des sciences fondamentales et cliniques à la FBM.
par Nathalie Isorce - Communication FBM