Le pneumocoque ou l’art de déjouer les antibiotiques
A l’origine de maladies graves, le pneumocoque tue chaque année 1 million de personnes dans le monde. Le Prof. Jan-Willem Veening et son équipe au Département de microbiologie fondamentale de l’UNIL élucident les stratégies mises au point par cette bactérie pathogène pour échapper aux antibiotiques et acquérir de nouvelles résistances. Leurs travaux, qui pourraient déboucher sur de nouvelles possibilités de traitement des infections à pneumocoque, sont à découvrir dans l’édition en ligne du 27 novembre 2018 de la revue «Cell Reports».
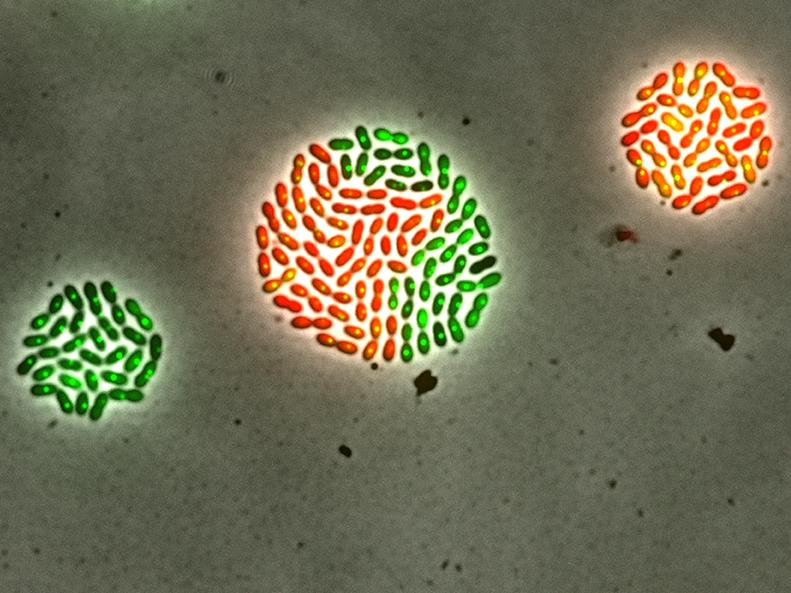
Communément appelé pneumocoque, Streptococcus pneumoniae est un pathogène humain qui colonise la région du pharynx. Il constitue l’une des principales causes bactériennes de morbidité et de mortalité à travers le monde. Présent chez 80% des enfants, généralement sans symptôme, il devient dangereux lorsque le système immunitaire s’affaiblit. Il peut alors être à l’origine de nombreuses maladies plus ou moins graves, allant de l’otite à la méningite, en passant par la pneumonie, voire une infection généralisée du sang (septicémie) pouvant conduire au décès du patient. Si la prise d’antibiotiques constitue une option thérapeutique, elle n’est pas toujours efficace en raison de la forte capacité d’adaptation de cette bactérie capable de développer des résistances.
Ce sont précisément les ruses mises au point par le pneumocoque pour déjouer les antibiotiques qui sont au cœur des travaux publiés dans Cell Reports. Afin d’élucider les diverses tactiques élaborées par ce fin stratège, les chercheurs du Département de microbiologie fondamentale (DMF) de la Faculté de biologie et de médecine de l’UNIL, en collaboration avec des microbiologistes du Centre for Synthetic Biology de l’Université de Groningue, aux Pays-Bas, ont utilisé des outils d’analyse novateurs combinant biologie synthétique et analyse d’une seule cellule.
Le microbe profite de l’ADN étranger pour se reprogrammer
Les scientifiques ont ainsi découvert qu’en assimilant et remaniant de l’ADN exogène, c’est-à-dire de l’ADN étranger qui provient de l’extérieur, la bactérie est capable de se reprogrammer de manière à développer de nouvelles résistances aux antibiotiques ainsi que d’augmenter sa virulence. «En nous appuyant sur des technologies de pointe, nous sommes parvenus à mettre en évidence le fait que certains antibiotiques favorisent l’acquisition d’ADN exogène, augmentant ainsi la propagation rapide de la résistance aux antibiotiques», détaille Arnau Domenech, premier assistant au sein du DMF et premier auteur de l’étude. «Ces antibiotiques modifient la morphologie intercellulaire, avec pour incidence la formation de longues chaînes de cellules. Ce phénotype – soit l’ensemble des traits observables d'un organisme – induit des changements au niveau de la communication entre bactéries, favorisant ainsi l’acquisition de l’ADN exogène.»
Vers de nouvelles stratégies thérapeutiques
Les recherches menées par les équipes lausannoise et néerlandaise peuvent avoir plusieurs implications: «D’une part, notre étude démontre l’importance d’une utilisation correcte des antibiotiques. Par exemple, en pratique, l’acide clavulanique, l’un des composés décrits dans notre travail, utilisé en association avec l’amoxicilline (Augmentin), constitue l’un des traitements antibiotiques les plus couramment utilisés contre les infections des voies respiratoires. Cependant, l’acide clavulanique est inutile pour le traitement spécifique des infections à pneumocoque. Notre étude suggère que, dans de tels cas, il est préférable de ne pas combiner l’acide clavulanique avec de l’amoxicilline, car cela favoriserait l’évolution du pneumocoque et potentialiserait le développement de la résistance aux antibiotiques», souligne Jan-Willem Veening, professeur ordinaire au DMF et directeur de l’étude. «D’autre part, une meilleure compréhension de la biologie de Streptococcus pneumoniae pourrait déboucher sur de nouvelles stratégies de traitement des infections à pneumocoque.»
par Manuela Palma de Figueiredo - Communication FBM